Los compuestos iónicos y moleculares: propiedades y estructura, así como su importancia, en diferentes ámbitos.
Procesos de desarrollo de aprendizajes:
Analiza la formación y estructura de compuestos iónicos y moleculares, a partir de las propiedades de la Tabla periódica.
¿Qué vamos aprender?
Conoceremos que el enlace químico se forma entre átomos de elementos diferentes o iguales, dando lugar a los compuestos iónicos o moleculares (covalentes). Así mismo conoceremos la importancia del estudio de las características de los compuestos con diferentes tipos de enlace, como también entenderemos que es necesario conocer la forma química por la que se forman los enlaces.
Compuestos iónicos y moleculares
Recordemos que los enlaces químicos son fuerzas que unen a los átomos entre sí para formar moléculas o compuestos.
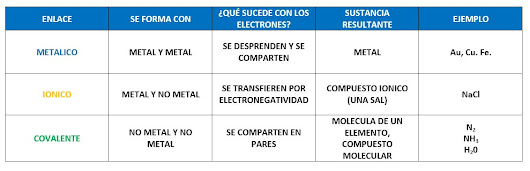
Ya sabemos que existen tres tipos de enlaces químicos
El enlace químico se lleva a cabo por la interacción de los electrones de valencia de los átomos involucrados.
Enlace iónico.
El enlace iónico se presenta con la atracción electrostática de átomos que poseen cargas eléctricas de signos contrarios (+, -) llamados iones, es este enlace un átomo pierde un electrón mientras que un segundo átomo lo gana; el resultado es que un átomo queda con carga positiva y otro con negativa, por lo que las cargas contrarias se atraerán formando el enlace.
Observa y toma nota del siguiente video:
Ver pagina 262 de tu libro de texto. Tabla de electronegatividad. Descargala e imprimela.
Para identificar un enlace iónico solo basta con saber la diferencia de electronegatividad entre los dos átomos unidos. si la diferencia de electronegatividad s mayor a 1.7 se tratará de un enlace iónico.
¿Qué es un ion? aniones y cationes
Los iones se forman cuando un átomo pierde o gana electrones. Los aniones tienen más electrones que protones y los cationes tienen un número de protones más alto.
Se denomina anión al ion que tiene carga eléctrica negativa
Se denomina catión al ion que tiene carga eléctrica positiva
Descarga la imagen dando click en ella e imprimimela, la vamos a necesitar para temas próximos.
Enlace covalente.
Observa con atención el siguiente video.
El enlace covalente es la unión química entre dos átomos que comparten electrones. Esto hace que los átomos se comporten como una unidad que llamamos molécula.
Los átomos interactúan entre sí por medio de los electrones más externos o de valencia formando enlaces.
El enlace covalente se puede clasificar atendiendo 3 aspectos.
1. Del numero de electrones compartidos.
Enlace covalente sencillo. Se comparten dos electrones.
Enlace covalente doble. se comparten 4 electrones.
Enlace covalente triple. Se comparten seis electrones.
2. Diferencia de electronegatividad.
Si entre los dos átomos enlazados la diferencia de electronegatividad va de 0 a 0.4 se trata de un enlace covalente no polar o puro. (la electronegatividad se toma de nuestro libro de texto de la tabla de pagina262.
Si la diferencia de electronegatividad va de 0.5 a 1.7 se trata de un enlace covalente polar
3. Numero de electrones aportado por átomo.
Si cada átomo aporta el mismo numero de electrones se trata de un enlace covalente normal.
Si un átomo aporta electrones y otro no, se trata de un enlace covalente coordinado o dativo. Observa con mucha atención.
Para recordar:
Actividad 4. busca tu nombre en el siguiente documento e identifica que tipo enlace químico se forma, reporta tu actividad en hojas blancas o de tu libreta (no olvides ponerle hoja de presentacion a tu actividad)
Formación de compuestos iónicos y moleculares.
En el enlace iónico, un átomo pierde un electrón mientras que un segundo átomo lo gana; el resultado es que un átomo queda con carga positiva y otro con carga negativa, por lo que las cargas contrarias se atraerán formando el enlace. Por otro lado, el enlace molecular o covalente se forma cuando dos átomos comparten al menos un par de electrones, en donde cada átomo aporta un electrón.
En la formación de los enlaces iónicos se puede observar la generación de cationes (átomos cargados positivamente) y aniones (átomos cargados negativamente), esto debido a que uno de los átomos tiene exceso de electrones en su capa de valencia, así que los cede a otro átomo con deficiencia de electrones; como los electrones son cargas negativas, uno de ellos queda cargado de manera negativa y el otro de forma positiva, lo que ocasiona que estos iones se atraigan uno a otro juntándose o enlazándose entre sí, causando que se formen redes de cientos de iones. Lo anterior imposibilita que se unan exclusivamente dos átomos para formar moléculas en comparación con el enlace covalente.
En la formación del enlace covalente dos átomos están deficientes de electrones en su capa de valencia, por lo que ninguno puede cederlos, así que ambos aportan un electrón para formar un enlace de manera que comparten esos dos electrones, es decir, no son del primer átomo ni del segundo, sino de ambos. Como este
proceso únicamente se puede llevar a cabo entre dos átomos, eso implica que se formen moléculas, que son aglomeraciones de átomos unidos químicamente por un enlace covalente. Ver figura página 168)
Estructura de los compuestos iónicos y moleculares
Como se mencionó anteriormente, los compuestos iónicos y moleculares o covalentes se forman por distintos procesos y, por ende, su estructura es diferente. Mientras que los compuestos iónicos forman redes con muchos átomos, los compuestos covalentes forman moléculas.
Los compuestos iónicos y los moleculares o covalentes son aquellos que tienen enlaces iónicos o covalentes, respectivamente. Es importante distinguirlos ya que, al formar moléculas o redes, cambian completamente sus propiedades.
Actividad 5. De los siguientes compuestos o elementos construye la estructura de Lewis y determina que tipo de enlace se forma.






















No hay comentarios.:
Publicar un comentario